Vous êtes dans : Accueil > traçabilité des dispositifs médicaux >
Traçabilité des dispositifs médicaux21 documents taggés
Concertation sur la traçabilité des DMI
28 septembre 2021 | DSIH | ActualitésL’Agence du numérique en santé a lancé une nouvelle concertation, du 16 septembre au 16 décembre 2021, sur le volet Traçabilité des dispositifs médicaux implantables en établissement de santé.
Un guide sur les systèmes d’information en stérilisation
12 juillet 2021 | DSIH | ActualitésLe 1er juillet, l’Anap a mis en ligne un nouveau guide sous la forme d’une boîte à outils destinés à améliorer la compréhension des spécificités et des exigences réglementaires, organisationnelles et techniques liées au système d’information pour sécuriser l’utilisation des dispositifs médicaux restérilisables.
Dispositifs médicaux : de nouvelles dispositions pour renforcer la sécurité des produits
01 juin 2021 | DSIH | ActualitésLe 26 mai 2021, un nouveau règlement européen sur les DM est entré en vigueur pour renforcer les prérequis nécessaires à l’obtention du marquage CE médical de même que les outils de traçabilité et de transparence.
Déconfinement et interopérabilité, un même combat ?
18 mai 2020 | DSIH | ActualitésLa crise sanitaire du Covid-19 a mis en évidence la nécessité de pouvoir communiquer à distance. Comment aurions-nous pu passer ces 54 jours de confinement sans Skype, Messenger, Teams, Zoom, WhatsApp… ? Imaginez un seul instant qu’un fournisseur d’accès Internet refuse purement et simplement ces technologies. Il aurait rapidement été contraint de s’adapter. L’interopérabilité dans la santé reproduit ce même schéma.
2es Trophées Innovation SantExpo
25 février 2020 | DSIH, Damien Dubois | ActualitésÀ l’occasion de SantExpo, du 26 au 28 mai, porte de Versailles à Paris, la deuxième édition des Trophées Innovation récompensera les applications et les projets innovants en santé.
GS1 dévoile son nouveau standard pour la traçabilité des essais cliniques
28 novembre 2019 | GS1 France | CommuniquéGS1, en collaboration avec plusieurs acteurs du secteur de la santé, présente un standard permettant une identification des produits de recherche dans les processus d’essais cliniques. Cette avancée répond à un besoin de meilleure identification et de traçabilité afin d’assurer la sécurité des patients.
Privilégier une solution complète pour gérer le parcours du patient en chirurgie
01 octobre 2019 | DSIH | ActualitésLa prise en charge d’un patient opéré fait intervenir de nombreux professionnels de santé. Elle est également soumise à de fortes contraintes réglementaires. Les établissements privilégient donc des solutions informatiques complètes, qui prennent en compte toutes les étapes de l’activité de chirurgie.
Traçabilité des dispositifs médicaux : restaurer la confiance
06 mai 2019 | DSIH, Pierre Derrouch | ActualitésSelon une note d’information(1) de la DGOS du 27 mars 2019 relative à la traçabilité des dispositifs médicaux implantables dans les établissements de santé et aux outils d’autoévaluation et d’accompagnement disponibles, l’informatisation du circuit du DMI est un prérequis essentiel à l’application de la réglementation en matière de traçabilité des DMI. La pression s’accentue sur les établissements.
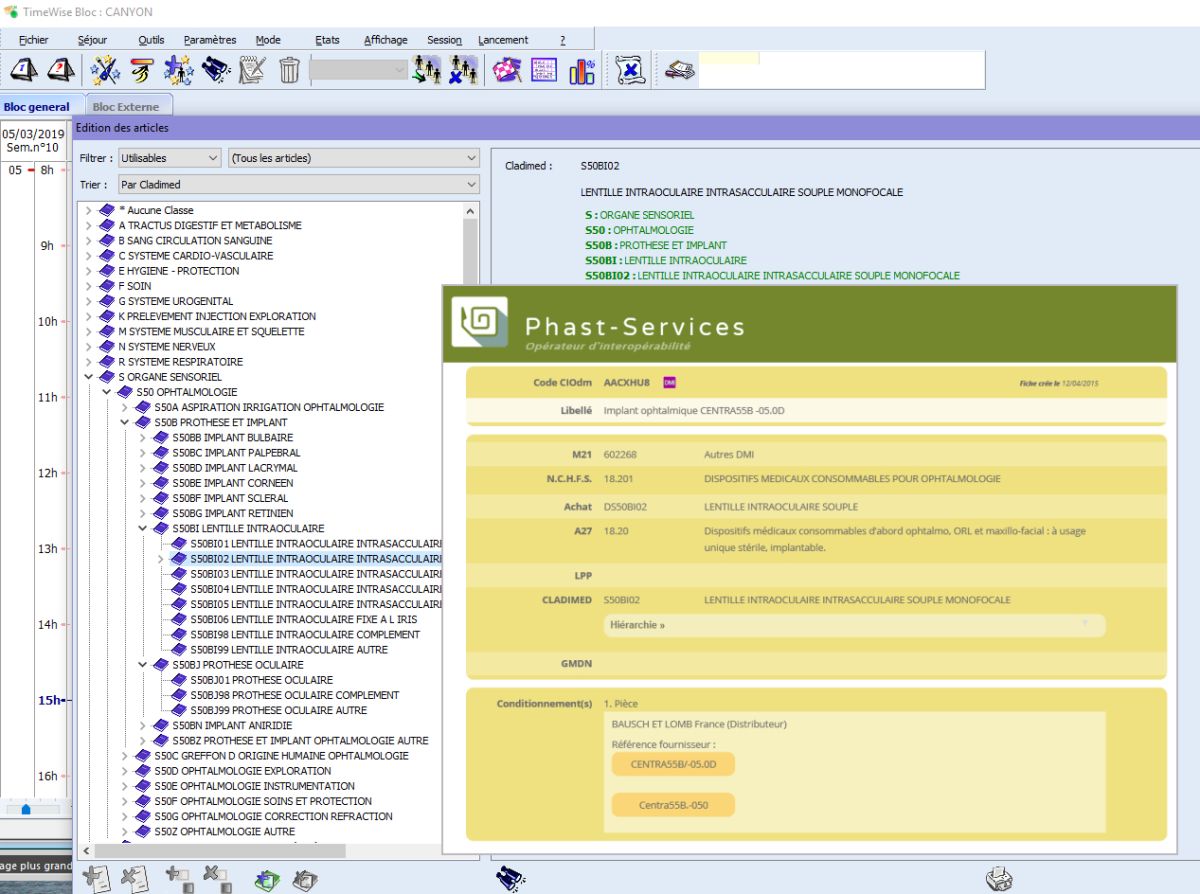
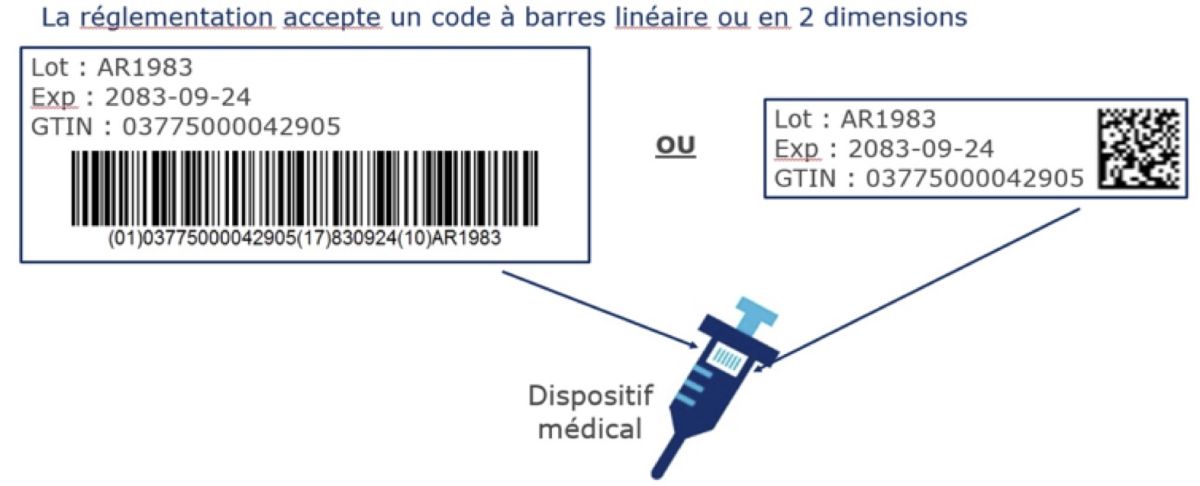
Traçabilité des dispositifs au bloc opératoire, TimeWise Bloc Pro déjà prêt
12 mars 2019 | DSIH, Pierre Derrouch | Actualités
Assurer la traçabilité des dispositifs médicaux implantables
08 octobre 2018 | DSIH | ActualitésPour répondre aux contraintes réglementaires, les établissements doivent mettre en œuvre une traçabilité complète des Dispositifs Médicaux Implantables (DMI), à chaque étape de leur circuit dans l’établissement.
GS1 France célèbre le World Standards Day
16 octobre 2017 | GS1 France | CommuniquéGS1, l’organisation mondiale de standardisation des échanges commerciaux, célèbre le World Standards Day (14 0ctobre 2017) et choisit pour cela de mettre en lumière l’usage des standards dans le secteur de la santé. Une utilisation synonyme de bénéfices majeurs à la fois pour les patients et les acteurs de la filière santé.
La réglementation relative aux dispositifs médicaux votée par le Parlement Européen
11 avril 2017 | GS1 | CommuniquéAnnoncé depuis plusieurs mois, le vote, par le Parlement Européen, de la réglementation européenne dispositifs médicaux est effectif depuis le 5 avril 2017. Elle intègre la notion nouvelle d’identifiant unique, également appelée en anglais « UDI » (Unique Device Identifier), permettant d’assurer une codification harmonisée et une meilleure traçabilité des dispositifs médicaux. Cette réglementation s’appuie sur les standards GS1 pour assurer son fonctionnement.
Bloc® sécurise le parcours du patient opéré
14 mars 2017 | DSIH, Bruno Benque | ActualitésUn projet d’informatisation de bloc opératoire doit prendre en compte la gestion du planning opératoire et la traçabilité des dispositifs médicaux. Les applications Bloc® et Sté®, de Computer Engineering, sont, dans ce cadre, des outils essentiels pour la sécurisation du parcours du patient opéré.
Pharma® répond aux évolutions du rôle des pharmaciens
08 mars 2016 | DSIH, BB | ActualitésLes équipes des Pharmacies à usage intérieur (PUI) sont confrontées à de nouvelles demandes de la part des autorités de tutelle et des services de gestion. Conciliation médicamenteuse, Groupements de coopération sanitaire (GCS), traçabilité des dispositifs médicaux, gestion des stocks et des multiples modes de dispensation entre différents sites… Pharma® s’adapte à l’ensemble de ces évolutions.
Traçabilité des dispositifs médicaux implantables dans les hôpitaux, le ministère de la Santé tire la sonnette d’alarme
23 février 2016 | DSIH, Bernard B | ActualitésLa DGOS a mené une enquête nationale dans les hôpitaux et cliniques. Des manquements sont pointés dans les SIH. Des corrections doivent être mises en œuvre sans plus tarder.
Comment assurer la traçabilité complète des Dispositifs Médicaux Implantables ?
13 octobre 2015 | DSIH, BB | ActualitésPour répondre aux contraintes réglementaires et au manuel de certification édité par la Haute Autorité de Santé, les établissements de santé doivent mettre en œuvre une traçabilité complète des Dispositifs Médicaux Implantables (DMI), à chaque étape de leur manipulation.
ATH Medical choisit le socle technologique d’InterSystems pour développer ses solutions intégrées de traçabilité des dispositifs médicaux
12 mars 2014 | PortisEd | CommuniquéEn moins de deux ans, ATH Medical est parvenue à développer une gamme de produits intégrés et interopérables de traçabilité des implants, des instruments chirurgicaux et des ancillaires, en s’appuyant sur la plateforme Ensemble.
Traça de Computer Engineering la solution pour la traçabilité des MDS et des DMI.
11 mars 2014 | Bruno Benque | ActualitésLes dernières évolutions du module de traçabilité de Computer Engineering permettent aux établissements de soins de répondre de manière simple et efficiente à toutes les contraintes réglementaires.
Pharma, la boîte à outils de la pharmacie à usage intérieur
10 février 2014 | DSIH | ActualitésGrâce à l'architecture modulaire de sa solution Pharma, Computer Engineering propose aux acteurs de la Pharmacie à Usage Intérieur (PUI) une boîte à outils capable de s'adapter à leurs besoins particuliers et couvrant tout le champ d'activités de la pharmacie.
Avec Traça, la traçabilité des DMI n'est plus une contrainte
08 avril 2013 | DSIH | ActualitésEn matière de traçabilité des Dispositifs Médicaux Implantables (DMI) les établissements de santé ont besoin d'une solution fluide et intégrée afin de répondre efficacement aux contraintes réglementaires. Ils peuvent désormais compter sur « Traça », de Computer Engineering, pour réaliser ce suivi.
Computer Engineering optimise la traçabilité
24 novembre 2011 | DSIH | ActualitésDix huit ans après le lancement des applications Bloc et Stérilisation, Computer Engineering répond toujours plus aux besoins des établissements de santé. Après la gestion du planning des salles opératoires et le suivi des stocks de produits consommables du bloc opératoire, les évolutions actuelles concernent la traçabilité des dispositifs médicaux implantables et la traçabilité des produits et instruments stérilisés dans l’établissement.
Les plus lus
e-santé
- 11/10/2022 - GIP Centre-Val de Loire e-Santé - (45)
Chargé(e) déploiement des usages
- 11/10/2022 - GIP Centre Val de Loire e-santé - (45)
Référent en Identitovigilance
- 11/10/2022 - GIP Centre Val de Loire e-Santé - (45)
Ingénieur de production
- 19/09/2022 - GIP Centre-Val de Loire e-Santé - (45)
Chargé(e) d’accompagnement Ségur/ SI ESMS